Según los resultados del estudio INFORM-1, publicados en la edición electrónica del 14 de octubre de The Lancet, un régimen compuesto por dos medicamentos orales que actúan directamente contra el virus de la hepatitis C (VHC) en fases diferentes de su ciclo vital puede inhibir la replicación del virus sin el empleo de interferón pegilado [IFN-PEG] y/o ribavirina [RBV]. La combinación del inhibidor de la proteasa del VHC danoprevir (RG7227 ó ITMN-191) y del inhibidor de la polimerasa RG7128 logró una reducción de, aproximadamente, 5log tanto en pacientes pretratados como en aquéllos que nunca antes habían recibido tratamiento contra la hepatitis C, y no provocó efectos secundarios graves en este estudio de escalado de dosis de 14 días de duración.
El tratamiento estándar anti-VHC con interferón pegilado y ribavirina no siempre es eficaz y se ve limitado por los efectos secundarios. Aunque manejables, éstos pueden llegar a ser tan graves que muchas personas deciden retrasar o interrumpir la terapia. Por consiguiente, urgen nuevos compuestos más eficaces, más fáciles de administrar y con menos efectos adversos. Afortunadamente, hay muchos nuevos medicamentos orales específicos contra el VHC en fase de desarrollo, pero al menos en los próximos años parece que deberán emplearse en combinación con la terapia actual: interferón pegilado, ribavirina o ambos. Se podría esperar regímenes anti-VHC sin el estándar actual de tratamiento cuando puedan combinarse varios medicamentos que actúen sobre distintas dianas del ciclo vital del virus hepático.
El INFORM-1 proporciona la prueba de concepto para un enfoque terapéutico contra el VHC según la cual la combinación de dos medicamentos orales con acción directa sobre el virus se puede administrar de forma segura sin la utilización del tratamiento estándar (interferón pegilado y/o ribavirina) y puede inhibir la replicación viral. Este ensayo, que está siendo realizado por Roche en colaboración con los laboratorios Intermune y Pharmasset, combina fármacos que estaban en fase I en el momento del estudio, lo que supone una diferencia respecto a la investigación más tradicional de medicamentos de acuerdo con la cual los estudios de combinación se efectúan en fases más avanzadas de su desarrollo o cuando ya han sido aprobados.
Se trata de un ensayo de fase I, a doble ciego, de escalado de dosis, en el que participaron 88 personas infectadas sólo por VHC, tanto pacientes sin experiencia en el tratamiento contra el virus hepático como personas que ya lo habían tomado anteriormente, entre ellas, un grupo que había tenido una respuesta nula a un ciclo de tratamiento previo (un descenso de la carga viral del VHC inferior a 1log a las 4 semanas o inferior a 2log a las 12 semanas de tratamiento).
Los participantes, inscritos en seis centros hospitalarios de Nueva Zelanda y Australia, tenían genotipo 1 del VHC (el que responde peor al tratamiento estándar) y fueron distribuidos aleatoriamente en 7 cohortes que tomaron combinaciones diversas de RG7128 (500 ó 1.000mg dos veces al día) y danoprevir (100 ó 200mg tres veces al día, o 600 ó 900mg dos veces al día) o bien placebo durante un período de 14 días (véase el diseño del estudio en la imagen). En total, 74 personas fueron distribuidas aleatoriamente a los grupos del estudio que probaban la combinación y 11, al grupo con placebo.
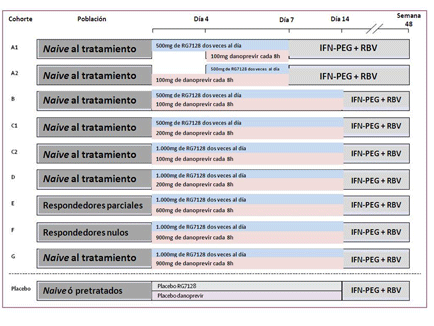
Tras completar el período de dosificación de los fármacos del ensayo y un período de lavado de 24 horas, los participantes continuaron tomando el tratamiento estándar contra la hepatitis C (180 μg/semana de interferón pegilado alfa-2a y 1.000 ó 1.200 mg/día de ribavirina ajustada al peso), excepto los pacientes incluidos en el grupo F (con respuesta nula a un tratamiento estándar anterior), que fueron desenmascarados tras la última evaluación del día 14 para que los investigadores pudieran decidir si debían empezar o no la terapia con interferón pegilado y ribavirina.
Como criterio de valoración principal del ensayo se estableció la determinación de los cambios en la carga viral del VHC desde el nivel basal hasta el día 14 en los pacientes que habían recibido durante 13 días la terapia combinada. Con anterioridad, se habían dado a conocer los resultados correspondientes a los tres últimos grupos en los que estaban incluidos los participantes que recibieron los regímenes con dosis más elevadas de los dos medicamentos tomados dos veces al día (E: pacientes pretratados; F: pacientes pretratados con respuesta nula; G: pacientes naive) [véase La Noticia del Día 13/11/2009]. El análisis, cuyos resultados ahora se publican, comprende a todos los participantes que completaron el tratamiento.
Los resultados muestran descensos medianos de la viremia desde el nivel basal hasta el día 14 que oscilaron entre 3,7 y 5,2log UI/mL en los grupos que recibieron la combinación de danoprevir y RG7128 durante 13 días.
Entre los participantes sin experiencia previa al tratamiento a los que se administraron las dosis más elevadas de ambos fármacos (grupo G: 900mg de danoprevir y 1.000mg de RG7128), el descenso mediano de la carga viral del VHC en el día 14 fue de 5,1log UI/mL. Entre las personas con respuesta nula a una terapia estándar anterior (grupo F) que recibieron la misma dosificación de los dos fármacos, se observó un descenso mediano similar: de 4,9log UI/mL. En los voluntarios que tomaron placebo, el descenso del ARN del VHC fue de sólo una mediana de 0,1log UI/mL.
Las reducciones de la carga viral fueron parecidas tanto en las personas con genotipo del VHC 1a como en aquéllas con genotipo 1b: 4,8 y 5,1log UI/mL, respectivamente.
En las cohortes que recibieron las dosis más altas de ambos fármacos, dos de 8 personas con respuesta nula a un tratamiento estándar anterior (grupo F) y cinco de 8 participantes naive a la terapia (grupo G) lograron reducir la carga viral del VHC hasta niveles indetectables (<15 UI/mL).
La combinación de los dos fármacos fue en general bien tolerada. Ningún participante interrumpió el tratamiento o redujo la dosis del fármaco por aspectos relacionados con la seguridad. No se advirtieron efectos secundarios graves relacionados con el tratamiento o anomalías de grado 3 ó 4 en los parámetros de laboratorio.
Tampoco se identificaron durante el ensayo indicios del desarrollo de resistencia a ninguno de los dos fármacos estudiados.
Sobre la base de estos hallazgos, los investigadores señalan en sus conclusiones que esta combinación oral de un inhibidor de la polimerasa y un inhibidor de la proteasa se muestra prometedora como tratamiento sin interferón pegilado contra la infección crónica por el VHC. A pesar de que los resultados evidencian que un enfoque terapéutico basado en la combinación de dos fármacos experimentales puede inhibir la replicación del VHC, los autores se mantienen cautelosos y afirman que, al tratarse de un estudio de fase 1 de prueba de concepto y de corta duración, no se puede mostrar que una combinación de fármacos contra el VHC sin interferón pegilado pueda erradicar el virus, o lo que es lo mismo, que el tratamiento alcance una respuesta virológica sostenida (carga viral del VHC indetectable 24 semanas después de la finalización del tratamiento). Además,
añaden que el estudio no inscribió a personas con cirrosis hepática, un grupo amplio e importante de pacientes que necesitan con más urgencia nuevos y más seguros tratamientos contra el VHC.
Por ello, arguyen que se debería continuar el desarrollo de la combinación del inhibidor de la proteasa danoprevir y del inhibidor de la polimerasa RG7128, dado su potencial como régimen terapéutico oral, sin interferón pegilado, para el tratamiento de la infección crónica por VHC.
Fuente: Elaboración propia / Hivandhepatitis.
Referencia: Gane EJ, Roberts SK, Stedman CA, et al. (INFORM-1 study team). Oral combination therapy with a nucleoside polymerase inhibitor (RG7128) and danoprevir for chronic hepatitis C genotype 1 infection (INFORM-1): a randomised, double-blind, placebo-controlled, dose-escalation trial. Lancet. October 14, 2010 (Epub ahead of print).
Suscríbete a nuestros boletines
Utiliza este formulario para suscribirte a nuestros boletines. Si tienes cualquier problema ponte en contacto con nosotros.
Al continuar, confirmas que has leído el aviso legal y aceptas la política de privacidad.







