Recientemente, la Red de Ensayos de Microbicidas (MTN, en sus siglas en inglés) ha dado a conocer que el Comité de Seguimiento de Datos y Seguridad (DSMB, en sus siglas en inglés) independiente del estudio VOICE decidió cancelar uno de los brazos del estudio (en el que se administraba tenofovir de forma oral) ante la evidencia de que incluso en el caso de que el ensayo siguiera adelante hasta su conclusión prevista, sería imposible que dicha intervención demostrara ningún efecto protector significativo frente al VIH, en comparación con un placebo.
El ensayo VOICE (Intervenciones Orales y Vaginales para Controlar la Epidemia, en sus siglas en inglés) estaba diseñado para comparar la aplicación de un gel microbicida con tenofovir y dos formas de profilaxis preexposición (PPrE) oral: una basada en el uso de tenofovir y otra, en un comprimido que combina tenofovir y emtricitabina (Truvada®). El estudio contaba con cinco grupos: En uno, las mujeres recibían un gel con tenofovir, en otro, un gel con placebo, en otro, tenofovir oral, en otro, Truvada® oral y, por último, otro más en el que recibía un placebo oral.
El estudio cuenta con la participación de 5.029 mujeres en 15 sedes de Uganda, Sudáfrica y Zimbabue. La decisión del DSMB se comunicará en la siguiente visita clínica de las participantes que reciben tenofovir por vía oral. Esto supondrá que unas 1.000 mujeres dejarán de tomar tenofovir por vía oral, pero el estudio seguirá en marcha para probar el gel microbicida con tenofovir y la administración oral de Truvada®. Los resultados finales se esperan para principios de 2013, una vez todas las participantes hayan completado, como mínimo, un año de seguimiento.
En relación con esta decisión, Mitchell Warren, director ejecutivo de AVAC (siglas en inglés de Coalición de Activismo en Vacunas contra el Sida) mostró su decepción por el hecho de que esto supondrá que el estudio VOICE sea incapaz de resolver la cuestión de si la administración oral de tenofovir previene o no la infección por VIH en mujeres. Sin embargo, también admite que es una buena noticia el hecho de que el ensayo sigue en marcha, probando la administración de un microbicida vaginal (cuya eficacia fue del 39% en el estudio CAPRISA 004) y de otra intervención de PPrE con Truvada®. Una de las cuestiones más importantes que quedan pendientes con urgencia es determinar qué estrategias preventivas funcionarán para las mujeres y VOICE seguirá constituyendo un ensayo clave para responder esta cuestión.
En los últimos meses se han hecho públicos los datos de distintos ensayos sobre profilaxis preexposición, que han arrojado unos resultados contradictorios. Así, mientras que en algunos estudios la intervención profiláctica arrojó unos niveles de eficacia notables, en otros (precisamente en los que participaba una población exclusivamente femenina), los resultados fueron decepcionantes.
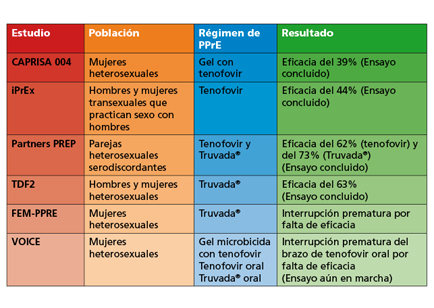
Como se puede observar en la tabla, la estrategia de PPrE basada en el uso de tenofovir resultó eficaz en el estudio Partners PREP, que anunció sus resultados en julio de 2011. En dicho estudio se comparó la profilaxis con este fármaco —oTruvada®— frente a un brazo de placebo y descubrió que el riesgo de infección se redujo en un 62% en el brazo de tenofovir y en un 73% en el de Truvada®. Dicho estudio contó con la participación de parejas heterosexuales serodiscordantes (véase La Noticia del Día 19/07/11).
Otro estudio, denominado TDF-2 y que contó tanto con hombres y mujeres en Botsuana, ha evidenciado que Truvada® redujo el riesgo de infección en un 63%. No obstante, el ensayo no estaba diseñado para evaluar si Truvada® resultaba igual de eficaz en la prevención de la infección en hombres y mujeres. Los resultados del estudio TDF-2 se anunciaron en julio de 2011 (véase La Noticia del Día 19/07/11).
Sin embargo, hace poco se anunciaron los resultados de otro estudio, denominado FEM-PREP, en el que participaban únicamente mujeres, que evidenciaron la falta de eficacia de una profilaxis preexposición basada en Truvada® (véase Actualización en Tratamientos 21/04/2011). El ensayo se interrumpió en abril de 2011 después de que el Comité de Seguimiento de Datos y Seguridad concluyera que no sería capaz de evidenciar ningún efecto preventivo del uso de Truvada® como PPrE, incluso aunque se ejecutase hasta su conclusión, al igual que ha ocurrido en el caso del estudio VOICE.
Fuente: Aidsmap / Elaboración propia
Referencia: Microbicide Trials Network. MTN statement on decision to discontinue use of oral tenofovir tablets in VOICE, a major HIV prevention study in women. Press release. 28 September 2011.
Suscríbete a nuestros boletines
Utiliza este formulario para suscribirte a nuestros boletines. Si tienes cualquier problema ponte en contacto con nosotros.
Al continuar, confirmas que has leído el aviso legal y aceptas la política de privacidad.







