A pesar de los grandes avances que se han producido en el tratamiento anti-VIH en los últimos años, siguen siendo necesarios nuevos fármacos o estrategias terapéuticas que resulten eficaces ante virus resistentes a los antirretrovirales disponibles en la actualidad y que ofrezcan también mejores perfiles de toxicidad. Por ello, están en desarrollo diversos compuestos de tipos ya existentes o de nuevas familias.
En esta edición de la CROI, destacamos los datos de eficacia del primer fármaco de una nueva clase. BMS-663068 es un profármaco del inhibidor del acoplamiento BMS-626529. Los estudios llevados a cabo en monoterapia con distintas dosis -con o sin ritonavir (Norvir®)- han mostrado descensos de carga viral acompañados de incrementos en el recuento de CD4. Su mecanismo de acción consiste en unirse directamente a la proteína gp120 de la superficie del VIH para bloquearla y así evitar que el virus entre en contacto con el receptor CD4 e infecte la célula. Al igual que los antagonistas del CCR5 y los inhibidores de la fusión, actúa fuera de la célula (véase imagen).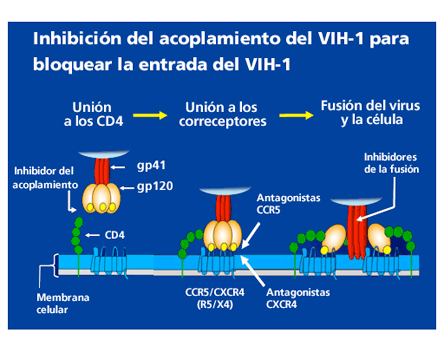 El estudio de prueba de concepto se realizó en 50 personas con VIH subtipo B naive o con al menos ocho semanas sin tratamiento. Todas tenían recuentos de CD4 por encima de las 200 células/mm3 y cargas virales superiores a 5.000 copias/mL. Fueron repartidas en cinco grupos para tomar diferentes dosis de BMS-663068 (600 o 1200mg) una o dos veces al día, con y sin ritonavir, durante un período de 8 días. Posteriormente, estas personas fueron seguidas hasta el día 50. En todos los grupos, se registraron descensos importantes de ARN del VIH de 1,59 a 1,77log, acompañados de un aumento en el recuento de linfocitos-T CD4 de entre 28 y 106 células/mm3.
El estudio de prueba de concepto se realizó en 50 personas con VIH subtipo B naive o con al menos ocho semanas sin tratamiento. Todas tenían recuentos de CD4 por encima de las 200 células/mm3 y cargas virales superiores a 5.000 copias/mL. Fueron repartidas en cinco grupos para tomar diferentes dosis de BMS-663068 (600 o 1200mg) una o dos veces al día, con y sin ritonavir, durante un período de 8 días. Posteriormente, estas personas fueron seguidas hasta el día 50. En todos los grupos, se registraron descensos importantes de ARN del VIH de 1,59 a 1,77log, acompañados de un aumento en el recuento de linfocitos-T CD4 de entre 28 y 106 células/mm3.
Durante el período del estudio, no se produjeron muertes ni se tuvo que interrumpir en ningún caso el tratamiento a causa de los efectos secundarios. El dolor de cabeza fue el acontecimiento adverso más común y se detectó en un 36% de pacientes. Según los investigadores, en los ensayos efectuados hasta la fecha, BMS-663068 se ha mostrado seguro y bien tolerado en general. Estos resultados avalan que prosiga su desarrollo. Además, sus características farmacodinámicas y farmacocinéticas apoyan que se prueben dosis inferiores -una o dos veces al día- y sin ritonavir. La compañía propietaria de la molécula, Bristol-Myers Squibb, ha anunciado en Boston que este mismo año iniciará un ensayo de fase IIb en pacientes con experiencia en el uso de antirretrovirales.
En cuanto a las clases ya existentes, sin duda, la que más candidatos en fases tempranas ha reunido en Boston es la familia de los inhibidores de la integrasa. Además de ViiV Healthcare y Gilead Sciences, otras compañías, así como equipos académicos independientes, trabajan para encontrar antirretrovirales de esta clase con características singulares que los diferencien de raltegravir (Isentress®) y de otros en fase ya avanzada de su desarrollo, como elvitegravir. La farmacéutica alemana Boehringer-Ingelheim ha identificado un nuevo tipo de inhibidores de la integrasa no catalíticos que empezará a probar en humanos a partir de ahora. Los primeros datos de laboratorio que ha ofrecido en esta conferencia la compañía sugieren que este nuevo tipo tiene actividad frente a virus resistentes a otros inhibidores de la integrasa y menos interacciones farmacológicas.
Por su parte, Gilead Sciences ensaya una nueva formulación del inhibidor de la transcriptasa inversa análogo de nucleótido tenofovir (Viread®, y coformulado en Truvada® y Atripla®), que proporciona mayores concentraciones intracelulares de difosfonato de tenofovir a las mismas dosis. En comparación con la formulación actual de tenofovir disoproxil fumarato, la monoterapia de 14 días con el profármaco GS-7340 a dosis más pequeñas (de 50 o 150mg) se ha asociado con descensos significativamente mayores de la carga viral y con menores exposiciones a tenofovir.
Más allá del desarrollo de nuevos fármacos antirretrovirales, o versiones mejoradas de los existentes, se están ensayando también estrategias innovadores, derivadas o no de la terapia genética, para prevenir o silenciar la infección de las células T por parte del VIH. Esta es una línea de investigación que puede aportar avances importantes de cara a una futura aproximación a la cura del VIH.
Dos trabajos presentados en esta edición de la CROI muestran cómo es posible modificar genéticamente las células T de un paciente para que se hagan resistentes a la infección. La idea se inspira en el conocimiento existente sobre los ‘controladores de elite’ (personas cuyas células del sistema inmunitario repelen al VIH por no tener correceptores CCR5 funcionales) y consiste en reproducir lo que ocurrió en el caso del conocido como ‛paciente de Berlín’, que eliminó el virus tras haber recibido células madre de un ‘controlador de élite’ para curar su leucemia. Ello propició que su sistema inmunitario se reconstruyera con células carentes de CCR5. Aplicar esta estrategia -trasplante de médula ósea- conlleva un alto riesgo para la vida del paciente, por lo que no procede hacerla extensiva a todas las personas con VIH. Por este motivo, grupos de científicos están investigando la modificación de células T del propio paciente (autólogas), en el laboratorio, para más tarde volver a introducirlas en su organismo.
Un estudio presentado en Boston por Jay Lalezari, del Instituto de Investigación Quest en San Francisco (EE UU), demuestra cómo usando una tecnología llamada ‛del dedo de zinc’, desarrollada por Sangamo BioSciences, se pueden obtener células con el CCR5 alterado. Las nucleasas de dedos de zinc se han convertido en reactivos útiles para la manipulación de los genomas de muchos organismos superiores. Aplicándola, en este caso, a células CD4 extraídas del mismo paciente, la nucleasa causa una fractura en el ADN de doble cadena del gen del CCR5. El proceso que se inicia entonces para reparar dicho gen altera de manera permanente la célula. Sin CCR5, el VIH -sobre todo cuando se trata de virus de tipo salvaje- no puede infectar.
En un pequeño ensayo abierto, un total de 6 personas con VIH en tratamiento y con carga viral indetectable, pero niveles de CD4 no muy altos (entre 200 y 500 células/mm3), se inscribieron y repartieron en dos cohortes para recibir o bien 10.000 millones o 20.000 millones de células. Un tercer grupo, actualmente en estudio, recibe 30.000 millones de células.
En el laboratorio, se expandieron células T autólogas con alteración del CCR5 con una tasa media de modificación de este correceptor del 25%. Las células resultantes se conocen con el nombre de SB-728-T. Las infusiones fueron bien toleradas y solo se dieron efectos secundarios leves, como un síndrome febril durante la infusión. Los participantes fueron seguidos de forma semanal durante un mes y mensualmente durante los 11 meses siguientes a la infusión.
En todos los pacientes funcionó el injerto, y en cinco de ellos se registraron aumentos importantes de CD4 al día 14 (de 35 a 1.038 células/mm3), con incrementos medios que se mantuvieron sostenidos durante todo el estudio (208, 86, 233, 911 y 210 células/mm3). En los cinco casos, también se normalizó el cociente CD4/CD8, situándose en valores por encima del 1.
Al cabo de 90 días, los niveles de células modificadas que se encontraron en la sangre periférica eran mucho más elevados de lo previsto: unas tres veces superiores. Asimismo, se hallaron células con alteración del CCR5 en la mucosa rectal, lo que indica que estas se habrían ido distribuyendo con normalidad a lo largo del intestino.
Como señaló el autor, es importante tener en cuenta que el mismo procedimiento implica la activación de las células CD4, lo que puede haber contribuido a su proliferación. Por otro lado, el paciente que no respondió presentaba altos niveles de anticuerpos contra el adenovirus que se usó como vector para introducir las células de nuevo en su organismo, lo que podría haber obstaculizado la alteración de CCR5.
El siguiente paso consistirá en probar este mismo procedimiento en personas con VIH y replicación viral para ver si con ello se consigue reducir la viremia. Para este fin, seleccionarán tanto a pacientes naive como a otros que no están respondiendo a la terapia antirretroviral.
Lalezari aseguró que estos resultados son la prueba de concepto que valida los hallazgos del caso del paciente de Berlín, pero también dejó claro que es demasiado pronto para relacionarlos con la curación. Si la terapia genética funciona, dijo este investigador, representará un importante avance en la supervivencia, ya que las células protegidas continuarán proliferando, mientras que aquellas que no han sido modificadas serán infectadas por el VIH y, por lo tanto, acabarán muriendo.
Por otra parte, el VIH puede utilizar otro correceptor de la superficie de la célula para entrar en esta, conocido con el nombre de CXCR4 y que se relaciona con una fase más avanzada de la infección. En la misma sesión en que se presentaron los resultados anteriores, otro grupo de investigadores, esta vez de la Universidad de Pennsylvania (EE UU), dio a conocer los detalles de un estudio que, usando la misma tecnología del dedo de zinc, buscó crear células resistentes a los virus que emplean preferentemente el correceptor CXCR4. Se trata de estudios de laboratorio y en un modelo de ratones con su sistema inmunitario humanizado, cuyos resultados también favorables avalan que esta línea de investigación siga adelante.
En sus conclusiones, los autores aseguran que estos resultados representan un paso importante hacia su objetivo a largo plazo de crear un sistema inmunitario resistente al VIH alterando genéticamente tanto el correceptor CCR5 como el CXCR4.
Fuente: Elaboración propia.
Referencias: Nowicka-Sans B, et al. Antiviral Activity of a New Small Molecule HIV-1 Attachment Inhibitor, BMS-626529, the Parent of BMS-663068. 18th Conference on Retroviruses and Opportunistic Infections, abstract 518, Boston, 2011.
Nettles R, at al. Pharmacodynamics, Safety, and Pharmacokinetics of BMS-663068: A Potentially First-in-class Oral HIV Attachment Inhibitor. 18th Conference on Retroviruses and Opportunistic Infections, abstract 49, Boston, 2011.
Fenwick C, et al. Identification of BI-C, a novel HIV-1 non-catalytic site integrase inhibitor. 18th Conference on Retroviruses and Opportunistic Infections, abstract 523, Boston, 2011.
Markowitz M et al. GS-7340 Demonstrates Greater Declines in HIV-1 RNA than TDF during 14 Days of Monotherapy in HIV-1-infected Subjects. 18th Conference on Retroviruses and Opportunistic Infections, abstract 152LB, Boston, 2011.
Lalezari J, et al. Successful and persistent engraftment of ZFN-M-R5-D autologous CD4 T Cells (SB-728-T) in aviremic HIV-infected subjects on HAART. 18th Conference on Retroviruses and Opportunistic Infections, abstract 46, Boston, 2011.
Wilen C, et al. Creating an HIV-resistant immune system: using CXCR4 ZFN to edit the human genome. 18th Conference on Retroviruses and Opportunistic Infections, abstract 47, Boston, 2011.
Suscríbete a nuestros boletines
Utiliza este formulario para suscribirte a nuestros boletines. Si tienes cualquier problema ponte en contacto con nosotros.
Al continuar, confirmas que has leído el aviso legal y aceptas la política de privacidad.







