Un ensayo francés, cuyos resultados se dieron a conocer recientemente en la XVIII Conferencia sobre Retrovirus e Infecciones Oportunistas (CROI), ha proporcionado más indicios acerca de un tema que, desde hace un tiempo, está generado un encendido debate a diferentes niveles y que tiene que ver con la equivalencia de dos de los fármacos más prescritos en la terapia de inicio: lamivudina y emtricitabina. Según los hallazgos de este último estudio, el empleo de emtricitabina en combinación con tenofovir se asocia de forma significativa con una reducción de la probabilidad de desarrollar la mutación M184V/I en el fracaso del tratamiento en comparación con la utilización de lamivudina y tenofovir.
Lamivudina (o 3TC, Epivir®; también en Kivexa® junto con abacavir; en Combivir®, con zidovudina, y en Trizivir®, con zidovudina y abacavir) y emtricitabina [o FTC, Emtriva®; también en Truvada® junto a tenofovir, y en Atripla®, con tenofovir y efavirenz] son fármacos antirretrovirales que pertenecen a la clase de los inhibidores de la transcriptasa inversa análogos de nucleósido (ITIN). En ocasiones, a ambos se los denomina fármacos ‘XTC’ como consecuencia de su presunta equivalencia en términos de estructura, actividad antiviral y de selección de la misma mutación de resistencia, la M184V/I, que puede comprometer por sí sola la respuesta a ambos fármacos y, además, conferir resistencia parcial a otros ITIN.
Dada la percepción de que lamivudina y emtricitabina son, en esencia, equivalentes, y debido a que el precio de la combinación lamivudina/tenofovir es inferior al de emtricitabina/tenofovir, resulta tentador favorecer el uso de la primera en un contexto de crisis económica y de restricciones presupuestarias como el actual. A esto se añade que la reciente aparición del genérico de lamivudina, con un precio de venta más competitivo, plantea la posibilidad de abaratar los costes, decoformular o romper las combinaciones de antirretrovirales a dosis fijas y administrar por separado los componentes para incorporar así la administración del nuevo genérico.
A la espera de conocer de forma empírica cómo la decoformulación de las combinaciones de antirretrovirales a dosis fijas podría afectar a la adhesión de los pacientes al tratamiento antirretroviral, cada vez van apareciendo más datos procedentes de ensayos clínicos que sugieren que ambas combinaciones de antirretrovirales podrían no ser exactamente equivalentes. En este sentido, los resultados de algunos estudios recientes apuntan a que ambos fármacos podrían presentar diferencias en cuanto a su potencia antiviral y a sus propiedades farmacocinéticas, por lo que éstas deberían tenerse en consideración por los médicos a la hora de prescribir una combinación que pudiera resultar subóptima para determinados pacientes.
Por ejemplo, un reciente estudio italiano que analizó de forma retrospectiva a 859 pacientes halló tasas de resistencia significativamente mayores en las pautas con lamivudina/tenofovir que con emtricitabina/tenofovir: M184V/I: 53% frente a 35% (cociente de probabilidades [CP]: 1,6; p= 0,031); K70R: 16% frente a 4% (CP: 4,0; p= 0,002); Y181C: 16% frente a 8% (CP: 3,8; p= 0,005); y T215F: 11% frente 4% (CP: 1,9; p= 0,020) [véase La Noticia del Día 01/06/2010]. De acuerdo con los investigadores italianos, estas diferencias observadas entre combinaciones en el perfil de resistencia podrían explicarse por la vida media intracelular más larga de emtricitabina respecto a lamivudina.
El estudio francés, cuyos resultados fueron presentados en la XVIII edición de la CROI, tuvo un objetivo similar al italiano, es decir, comparar de forma retrospectiva la frecuencia y la cinética de la selección de mutaciones de resistencia tras un primer episodio de fracaso virológico de un régimen antirretroviral que incluía la pauta emtricitabina/tenofovir o lamivudina/tenofovir.
Se inscribió en el análisis un total de 880 pacientes que recibían seguimiento clínico en dos grandes centros hospitalarios franceses. De estos 880, un total de 150 pacientes (17%) estaban infectados por VIH-1 subtipo no B. En todas las personas que participaron en el estudio se registró por primera vez fracaso virológico tomando tratamiento antirretroviral y después de haber estado, como mínimo, seis meses con carga viral indetectable. Los regímenes antirretrovirales que recibían los pacientes en el momento del fracaso incluyeron, además de las combinaciones de nucleósidos anteriormente señaladas, el no análogo de nucleósido [ITINN] efavirenz (Sustiva®) o un inhibidor de la proteasa potenciado por ritonavir (IP/r; Kaletra® o Reyataz®/Norvir®):
- Lamivudina + tenofovir + efavirenz (n= 178)
- Lamivudina + tenofovir + IP/r (n= 167)
- Emtricitabina + tenofovir + efavirenz (n= 257)
- Emtricitabina + tenofovir + IP/r (n= 278)
Esto es, cuando se produjo el fracaso virológico, un total de 345 pacientes (39,20%) estaban tomando un régimen antirretroviral que incluyó la combinación lamivudina/tenofovir, y 535 (60,80%), la pauta de emtricitabina/tenofovir. Todas las personas que participaron en el estudio disponían en su historial clínico de los resultados de un test de resistencia genotípica realizado tras constatar el fracaso virológico (con niveles superiores a 200 copias/mL).
Los dos grupos de pacientes (el de lamivudina/tenofovir frente al de emtricitabina/tenofovir) presentaban características semejantes en lo que se refiere a la mediana de la carga viral y el recuento de células CD4 basales; a los cambios medianos en la viremia y en el recuento de CD4 desde el nivel basal hasta el momento del fracaso virológico; y a la mediana de tiempo transcurrido hasta que tuvo lugar dicho fracaso.
Los resultados del análisis genotípico muestran una prevalencia de la mutación M184V/I significativamente más baja en pacientes en los que fracasó la combinación emtricitabina/tenofovir (24%) que en aquellos en los que fracasó la pauta de lamivudina/tenofovir (51%), en ambos casos tomadas junto con efavirenz (p <0,0001). No se observaron diferencias significativas entre los dos grupos por lo que respecta a la selección de mutaciones de resistencia a los ITINN (55% y 62%, respectivamente).
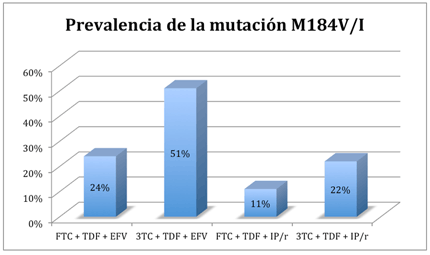
En los pacientes que recibieron un inhibidor de la proteasa potenciado por ritonavir pudo advertirse el mismo efecto significativo: en un 11% de las personas que tomaron emtricitabina/tenofovir y en un 22% de aquellas que recibieron lamivudina/emtricitabina pudo detectarse la mutación M184V/I (p= 0,002). No se apreciaron diferencias significativas entre los dos grupos en cuanto a la selección de mutaciones de resistencia a la proteasa (6% y 9%, de forma respectiva).
Según el análisis de los investigadores, de entre todos los factores posibles (viremia basal, subtipo de VIH, recuento nadir y basal de CD4, duración del fracaso virológico, carga viral en el momento del fracaso, uso de 3TC frente a FTC, empleo de ITINN frente a IP/r), solo se asociaron con el desarrollo de la mutación M184V/I el empleo de 3TC, ITINN y el nivel de la carga viral en el momento del fracaso virológico.
En sus conclusiones, los autores señalan que los hallazgos de su estudio, que muestran que la utilización de emtricitabina se relaciona de forma significativa con una disminución de la probabilidad de desarrollar la mutación M184V/I en el fracaso de tratamiento en comparación con lamivudina, son coincidentes con los datos de otros ensayos independientes publicados recientemente, como por ejemplo el análisis del doctor R. Maserati, publicado en abril de 2010 en la revista AIDS.
Además, de acuerdo con los investigadores, este estudio subraya la importancia de identificar combinaciones de antirretrovirales que puedan minimizar el desarrollo de resistencia a los fármacos, una estrategia que podría resultar útil para todos los contextos clínicos, pero sobre todo en aquellos países de recursos limitados donde existe un escaso acceso a las pruebas de carga viral y de resistencia genotípica.
Con todo, al tratarse de un ensayo retrospectivo y debido a las limitaciones de este tipo de análisis, debe tomarse como una sugerencia el combinar preferentemente tenofovir con emtricitabina en lugar de hacerlo con lamivudina. Serán necesarios amplios estudios de cohorte prospectivos que confirmen el potencial aumento del riesgo de mutaciones de resistencia en el momento del fracaso con lamivudina/tenofovir frente a emtricitabina/tenofovir para que la sugerencia pueda convertirse, en la práctica clínica, en una recomendación basada en un máximo nivel de evidencia.
Fuente: Elaboración propia.
Referencia: Marcelin AG, Charpentier C, Wirden M. Resistance profiles of emtricitabine and lamivudine in tenofovir-containing regimens. 18th Conference on Retroviruses and Opportunistic Infections (CROI 2011). Boston. February 27-March 2, 2011. Abstract 617.
Suscríbete a nuestros boletines
Utiliza este formulario para suscribirte a nuestros boletines. Si tienes cualquier problema ponte en contacto con nosotros.
Al continuar, confirmas que has leído el aviso legal y aceptas la política de privacidad.







